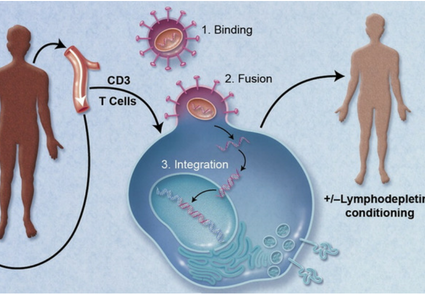
La terapia CAR-T consiste en un tipo de tratamiento para el que se cambian las células T de un paciente, mediate técnicas avanzadas de laboratorio, a fin de que se unan a las células cancerosas y las destruyan. Actualmente la terpia CAR-T se considera experimental o en estudio para el tratamiento de algunos tipos de cáncer. Sin embargo un estudio publicado en la revista Nature puede abrir las puertas a que esta terapia sea investigada con mayor frecuencia para lograr ser implementada en más centros de salud alrededor del mundo.
La aplicación de la terapia celular basada en linfocitos portadores de receptores quiméricos para el antígeno (CAR-T) en un paciente con leucemia linfocítica crónica ha tenido un efecto positivo, de acuerdo a un grupo de trabajo de la Universidad de Pennsylvania.
En este estudio se analiza que la generación de CAR-T a partir de los linfocitos del paciente incluye la integración en el genoma celular de un vector lentiviral portador del receptor quimérico. A pesar de los recientes éxitos de esta terapia, el grado de expansión y de persistencia de los CAR-T es limitada.
En el paciente tratado se observó actividad anti-tumoral en la sangre, en la médula ósea y en los ganglios linfáticos, con remisión completa de la enfermedad.
Los investigadores observaron durante el nivel máximo de respuesta, el 94% de los CAR-T tenían su origen en un único clon en el que la inserción lentiviral había causado una disrupción en el gen de la metilcitosina dioxigenasa (TET2), un gen relacionado con la regulación de la proliferación de las células sanguíneas.
En la fase de máxima actividad anti-tumoral, los CAR-T deficientes en el gen TET2 mostraron un perfil epigenético consistente con una diferenciación celular alterada y un fenotipo característico de los linfocitos T centrales de memoria.
El estudio concluye que la progenie de una sola célula CAR-T induce la remisión de la leucemia y que la modificación de TET2 puede ser útil para mejorar la inmunoterapia.
Fuentes:
Artículo de nature: Disruption of TET2 promotes the therapeutic efficacy of CD19-targeted T cells






